發(fā)布時(shí)間:2023-06-30 瀏覽量:0
外泌體是由大多數(shù)細(xì)胞分泌的納米級(jí)囊泡,具有磷脂雙層結(jié)構(gòu)。外泌體含有DNA、小RNA、蛋白質(zhì)和其他可以攜帶蛋白質(zhì)和核酸并參與細(xì)胞間通訊的物質(zhì)。T細(xì)胞是適應(yīng)性免疫不可或缺的組成部分,T細(xì)胞來源的外泌體在細(xì)胞間信號(hào)傳導(dǎo),特別是腫瘤免疫應(yīng)答中發(fā)揮著新的作用。

有研究表明,外泌體是將蛋白質(zhì)、脂質(zhì)和核酸轉(zhuǎn)運(yùn)到靶細(xì)胞的細(xì)胞間連接點(diǎn),在各種生物過程(如血管生成、抗原呈遞、細(xì)胞凋亡和炎癥)中發(fā)揮作用,并可作為疾病的診斷和治療工具。外泌體還可以參與各種病理生理過程,如組織修復(fù)、免疫反應(yīng)、炎癥,腫瘤生長(zhǎng)和轉(zhuǎn)移。T淋巴細(xì)胞來源于骨髓中的多能干細(xì)胞。在人類生命的胚胎和初級(jí)階段,骨髓中的多能干細(xì)胞或前體T細(xì)胞在胸腺激素的誘導(dǎo)下遷移到胸腺并成熟為具有免疫活性的T細(xì)胞。
免疫細(xì)胞通過分泌外泌體參與細(xì)胞通訊。在免疫細(xì)胞來源的外泌體中,有報(bào)道稱T細(xì)胞來源的外泌體通過模仿親代細(xì)胞的作用參與癌癥免疫治療中的抗腫瘤作用。T細(xì)胞上調(diào)和下調(diào)外泌體的產(chǎn)生是調(diào)節(jié)腫瘤免疫應(yīng)答的新方法。
1 外泌體的生物發(fā)生和分泌
外泌體是在多泡體(MVBs)成熟過程中由內(nèi)體膜向內(nèi)出芽形成的腔內(nèi)囊泡(ILVs)。隨后,MVBs與質(zhì)膜融合以外泌體形式釋放所含ILVs,或與溶酶體或自噬體融合降解 (圖1)。
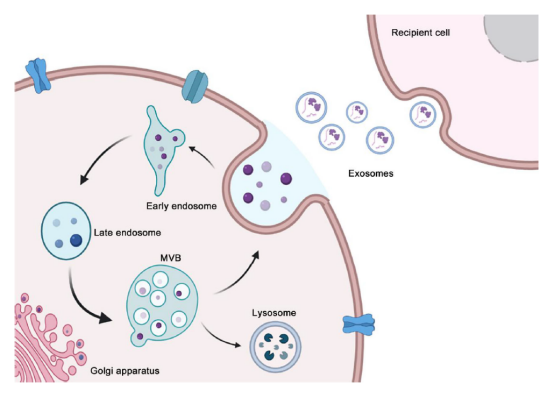
△外泌體的發(fā)生和分泌過程
外泌體的生物發(fā)生始于早期內(nèi)吞作用在質(zhì)膜處形成內(nèi)泌體,然后LSEs的質(zhì)膜內(nèi)陷形成ILVs,最終作為外泌體分泌。最后,MVBs與質(zhì)膜融合釋放外泌體。胞外體起源于質(zhì)膜的外出芽和裂變,隨后,新生的胞外體被釋放到細(xì)胞外空間。
外泌體的產(chǎn)生是復(fù)雜的,通常取決于宿主和親本細(xì)胞的類型以及細(xì)胞接受的其他刺激。此外,外泌體內(nèi)含物的性質(zhì)和含量是特異性的,經(jīng)常受到母細(xì)胞的生理或病理狀態(tài)、調(diào)節(jié)其產(chǎn)生和釋放的刺激以及促進(jìn)其產(chǎn)生的分子機(jī)制的影響。
2 T細(xì)胞源性外泌體
T細(xì)胞可產(chǎn)生反映其特性的外泌體,如直接殺死靶細(xì)胞,協(xié)助或抑制B細(xì)胞產(chǎn)生抗體,對(duì)特定抗原和有絲分裂原作出反應(yīng),產(chǎn)生細(xì)胞因子,從而以旁分泌和自分泌形式為免疫細(xì)胞發(fā)揮功能創(chuàng)造最佳的微環(huán)境。
T細(xì)胞衍生的外泌體可以激活其他免疫細(xì)胞,抑制免疫反應(yīng)。
在近期一項(xiàng)研究中,研究人員將白細(xì)胞介素(IL)-2通過柔性連接體連接到血小板衍生生長(zhǎng)因子受體的跨膜結(jié)構(gòu)域,然后將該基因整合到慢病毒中,用于Jurkat細(xì)胞感染。感染的Jurkat細(xì)胞分泌IL -2外泌體,IL -2外泌體中miR-181a-3p和miR-223-3p的表達(dá)相對(duì)于未處理的外泌體有顯著變化。miRNAs增加了黑色素瘤中CD8+ T細(xì)胞的活性,降低了程序性死亡配體1 (PD-L1)的表達(dá),從而增加了對(duì)CD8+ T細(xì)胞介導(dǎo)的細(xì)胞毒性的敏感性,T細(xì)胞可以根據(jù)其激活狀態(tài)調(diào)節(jié)不同外泌體亞群的釋放。
2.1 CD8+ T細(xì)胞衍生的外泌體
CD8+ T細(xì)胞是細(xì)胞毒性T淋巴細(xì)胞(CTL),是白細(xì)胞的一個(gè)亞群,分泌各種細(xì)胞因子特異性殺死靶細(xì)胞。它可以清除病毒感染細(xì)胞、腫瘤細(xì)胞和其他細(xì)胞。研究表明,CD8+ T細(xì)胞衍生的外泌體介導(dǎo)免疫細(xì)胞和腫瘤細(xì)胞之間的信息交換,從而調(diào)節(jié)腫瘤的發(fā)展。被腫瘤抗原完全激活的CD8+ CTL通過分泌外泌體增強(qiáng)低親和力CD8+ T細(xì)胞的激活,從而參與腫瘤殺傷過程。
具體來說,活化的CD8+ T細(xì)胞來源的外泌體通過降低dc中的MHC-I和黑色素瘤模型中的CD8+ T細(xì)胞活性來抑制抗腫瘤作用。CD8+ T細(xì)胞衍生的外泌體除了通過介導(dǎo)免疫細(xì)胞間的信息交換參與腫瘤生長(zhǎng)調(diào)控外,還直接抑制腫瘤進(jìn)展。此外,除了T細(xì)胞衍生的外泌體在免疫調(diào)節(jié)中的作用外,CD8+ T細(xì)胞還可以通過外泌體介導(dǎo)的間充質(zhì)腫瘤基質(zhì)細(xì)胞的消耗來抑制腫瘤的進(jìn)展。
2.2 CD4+ T細(xì)胞來源的外泌體
CD4+ T細(xì)胞通過產(chǎn)生細(xì)胞因子與NK細(xì)胞、巨噬細(xì)胞和CD8+ T細(xì)胞等其他細(xì)胞相互作用。研究表明,CD4+ T細(xì)胞衍生的外泌體增加了CD8+ T細(xì)胞的抗腫瘤反應(yīng),而不影響Tregs,從而抑制黑色素瘤的生長(zhǎng)。除了影響細(xì)胞免疫外,CD4+ T細(xì)胞衍生的外泌體還參與調(diào)節(jié)體液免疫,接種乙型肝炎表面抗原(HBsAg)疫苗的小鼠對(duì)CD4+ T細(xì)胞來源的外泌體表現(xiàn)出更強(qiáng)的體液免疫反應(yīng),表明血清中乙型肝炎表面抗體(HBsAb)水平更高。此外,CD4+ T細(xì)胞衍生的外泌體在體外B細(xì)胞應(yīng)答中發(fā)揮重要作用,顯著促進(jìn)B細(xì)胞活化、增殖和抗體產(chǎn)生。
2.3 Treg衍生外泌體
Treg是一組負(fù)性調(diào)節(jié)機(jī)體免疫反應(yīng)的淋巴細(xì)胞,參與腫瘤細(xì)胞的免疫應(yīng)答并發(fā)揮重要作用。由于Treg衍生的外泌體具有顯著的免疫抑制作用,越來越多的研究關(guān)注其在腫瘤免疫逃逸中的作用。據(jù)報(bào)道,Tregs比其他T細(xì)胞在表面分泌更多表達(dá)CD25、CTLA-4和CD73的外泌體。表達(dá)CD73的外泌體通過產(chǎn)生腺苷發(fā)揮免疫抑制功能,腺苷在抗炎反應(yīng)中起重要作用。
在最近的一項(xiàng)I期臨床試驗(yàn)中,18名頭頸部鱗狀細(xì)胞癌患者接受了西妥昔單抗、易普利姆單抗和放射治療的聯(lián)合治療,對(duì)Treg衍生外泌體進(jìn)行了連續(xù)監(jiān)測(cè),發(fā)現(xiàn)Treg衍生外泌體比基線水平增加,支持Treg衍生外泌體作為非侵入性腫瘤和免疫細(xì)胞生物標(biāo)志物在癌癥中的潛在作用。
3 嵌合抗原受體T細(xì)胞衍生外泌體
CAR-T療法不可避免地會(huì)產(chǎn)生細(xì)胞因子釋放綜合征、神經(jīng)毒性、器官衰竭等副作用。CAR-T細(xì)胞衍生的外泌體(下圖)可以降低CAR-T治療的細(xì)胞毒性,并穿過血腦屏障和血腫瘤屏障。CAR-T細(xì)胞衍生的外泌體表達(dá)高水平的細(xì)胞毒性分子(FasL、Apo2L、穿孔素等),使其成為有效的載體,為攜帶同源抗原的靶向腫瘤細(xì)胞提供促凋亡線索。
此外,一些臨床前研究證實(shí),CAR-T細(xì)胞衍生的外泌體對(duì)包括TNBC和肺癌在內(nèi)的實(shí)體腫瘤具有抑制作用,并且相對(duì)安全。活化的CAR-T細(xì)胞可分泌外泌體在實(shí)體瘤中發(fā)揮作用,并可影響腫瘤的免疫微環(huán)境。
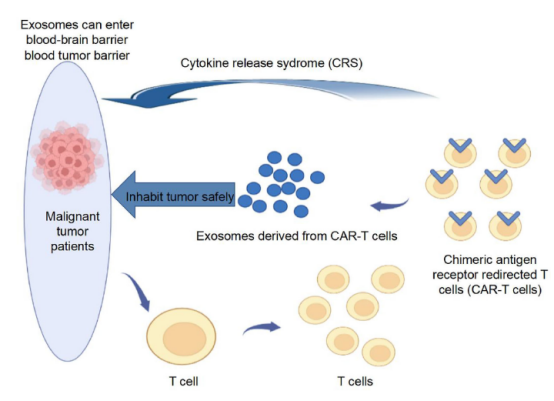
△CAR-T細(xì)胞衍生的外泌體用于腫瘤治療
CAR-T細(xì)胞衍生的外泌體表達(dá)高水平的細(xì)胞毒性分子,使其成為向攜帶同源抗原的靶向腫瘤細(xì)胞提供促凋亡線索的有效載體。
本文介紹了CD8+ T細(xì)胞、CD4+ T細(xì)胞和Treg來源的外泌體在腫瘤免疫調(diào)節(jié)中的作用。然而,對(duì)T細(xì)胞來源的外泌體的研究仍處于不斷探索階段,在T細(xì)胞衍生的外泌體從實(shí)驗(yàn)室向臨床過渡之前,還有許多障礙需要克服。
1.外泌體的純化和表征方法因?qū)嶒?yàn)室而異
不同的方法可能會(huì)混淆外泌體的亞群和理化性質(zhì)。因此,研究人員需要參考國際細(xì)胞外囊泡協(xié)會(huì),以及外泌體分離、純化和用于治療的標(biāo)準(zhǔn)化工作。
2.第二個(gè)問題是外泌體的產(chǎn)生
從細(xì)胞中提取的外泌體數(shù)量很少,往往難以滿足藥物遞送的要求。因此,要繼續(xù)擴(kuò)大外泌體的應(yīng)用,需要大規(guī)模的生產(chǎn)模式。
3.外泌體修飾或載藥后的穩(wěn)定性和毒性
有待進(jìn)一步探索,特別是作為腫瘤納米醫(yī)學(xué)應(yīng)用的載體。這些發(fā)現(xiàn)將促進(jìn)外泌體的臨床轉(zhuǎn)化。最佳的外泌體治療候選有效載荷目前尚無定論,需要在未來進(jìn)一步探索。
外泌體與其他藥物傳遞系統(tǒng)相比具有許多優(yōu)點(diǎn),特別是穩(wěn)定性高、免疫原性低、能夠避免單核吞噬細(xì)胞的清除、生物相容性好、生物活性高、靶向效率高。我們相信,在科學(xué)家、醫(yī)生等多方人員的共同努力下,基于T細(xì)胞的外泌體或可在未來成為對(duì)抗腫瘤的有力工具。
參考資料
[1] Zhou Q, Wei S, Wang H, Li Y, Fan S, Cao Y, Wang C. T cell-derived exosomes in tumor immune modulation and immunotherapy. Front Immunol. 2023 Apr 20;14:1130033. doi: 10.3389/fimmu.2023.1130033. PMID: 37153615; PMCID: PMC10157026.



