發布時間:2023-09-04 瀏覽量:0

近日,在《Stem Cell Research & Therapy》雜志上的一篇文章中,研究人員表示,來源于間充質干細胞的外泌體(MSC-Exos)是一種非常有前途的無細胞治療工具。外泌體可以作為一種新的策略來治療阿爾茨海默病、I 型糖尿病、癌癥、慢性腎臟疾病,甚至未來皮膚上的痤瘡疤痕。

這項研究結果也讓人們對間充質干細胞外泌體在疾病方向的臨床應用前景有了更多的認識。
隨著外泌體研究的不斷深入,它已經涉及多種疾病、問題領域。間充質干細胞來源的外泌體(MSC-EXOs)攜帶間充質干細胞的生物活性物質,因而可能具備與間充質干細胞相似的應用效果(如促進再生、抗炎、免疫調節等),同時可避免細胞應用的潛在風險。從現有的研究來看,除了上述所提到的疾病方向,間充質干細胞來源的外泌體對神經系統疾病、自身免疫病、癌癥、缺血性心臟病、肺損傷、肝纖維化等多種疾病也有一定效果。
下面是一些間充質干細胞外泌體的臨床應用研究案例。
糖尿病方向的應用研究
當前已有研究將外泌體引入糖尿病領域。研究表明,外泌體參與了糖尿病及其相關并發癥的發生與發展,它不僅可以作為糖尿病早期診斷和分期的生物學標記,還可作為糖尿病治療的靶點,更重要的是可以監測糖尿病患者對治療的反應,為實施糖尿病的個體化治療提供依據。
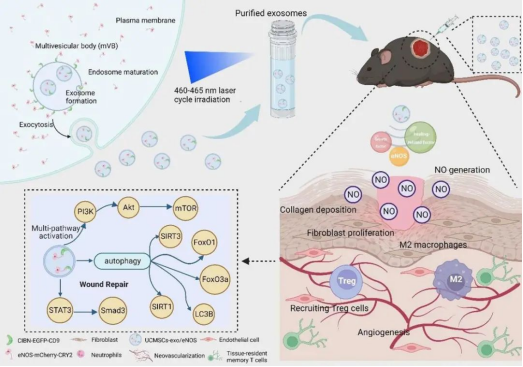
糖尿病患者由于基礎疾病的存在促進了慢性傷口的形成。一些研究也表明間充質干細胞源性外泌體在促進傷口愈合方面具有一定潛力,有研究人員通過基因工程和光遺傳學技術,獲得大量負載內皮型一氧化氮合酶(eNOS)的間充質干細胞源性外泌體,觀察其對成纖維細胞和血管內皮細胞生物學功能的影響。實驗結果表明,MSC-EXOs/eNOS可明顯改善高糖處理后細胞的生物學功能,促進了細胞的增殖和遷移,同時減少了氧化應激誘導的炎性因子表達和細胞凋亡。動物實驗結果顯示,MSC-EXOs/eNOS顯著提高了糖尿病小鼠的創面閉合率,促進了血管新生和基質重塑。此外,MSC-EXOs/eNOS還可以改善創面炎癥狀態、調節免疫微環境,進而發揮促進組織修復的作用。
心腦血管方向的應用研究
干細胞外泌體的心臟保護機制已成為研究熱點。越來越多的研究證實,干細胞源性外泌體具有與干細胞相似的心臟保護功能,能促進血管生成,減少細胞凋亡,減少應激帶來的損傷。外泌體具有較好的穩定性,較少引起受體細胞的突變以及免疫排斥反應,有望成為治療心血管疾病的有效方法。
2015年的一項研究發現,間充質干細胞源性外泌體移植后能顯著提高心肌細胞的存活率,并能抗心肌細胞損傷,促進新生血管形成,改善心臟功能。其他研究也證實了間充質干細胞源性外泌體具有抗炎、抗心肌細胞凋亡、促進心肌細胞再生的作用。
另外外泌體在多種腦損傷模型中展現出神經保護作用,今天要分享的是一項關于新生兒缺氧缺血性腦病的研究案例。
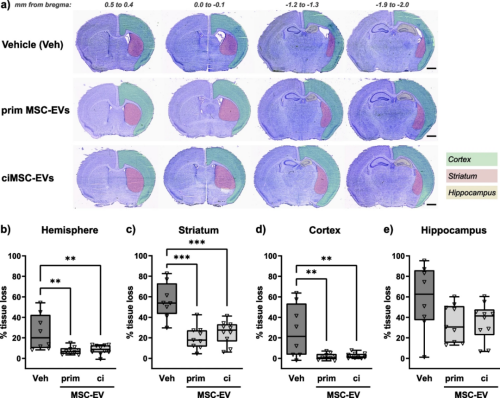
為實現間充質干細胞源性外泌體的規模化制備,一項研究中在小鼠腦損傷模型中對ciMSC來源外泌體的神經保護作用進行了研究。
通過對腦萎縮、局灶性腦萎縮、神經炎性反應和再生、外周炎癥介質等多個指標進行比較,研究人員發現ciMSC來源外泌體可有效保護新生小鼠免于缺氧所致的腦組織萎縮,其作用機制與減少小膠質細胞的激活和星形膠質細胞的增生、減少內皮細胞的激活、減少白細胞的浸潤緊密相關,而上述變化則與腦組織中促炎細胞因子的下調和抗炎細胞因子的上調有關。由此研究人員得出結論,ciMSC來源外泌體通過抑制神經炎癥和促進神經再生發揮保護作用。
皮膚問題方向的應用研究
近年來,研究人員將外泌體與皮膚問題聯系起來,發現外泌體不僅參與皮膚生理、病理過程,如調節皮膚微環境中促炎細胞因子分泌,促進皮膚缺損處血管新生及膠原沉積,以及調節皮膚成纖維細胞增殖分化,同時還在皮膚微環境發生病變時發揮特異性信息傳遞作用,進而促使增生性瘢痕、皮膚硬化及皮膚黑色素瘤等皮膚疾病的發生。
最近有學者發現外泌體可用于皮膚創傷后的傷口愈合,且能有效防治增生性瘢痕、黑色素瘤等皮膚疾病,為外泌體的應用研究提供了一個嶄新的方向。
另外近期外泌體在改善肌膚色素沉著方面,也表現出了一定的效果,韓國ExoCoBio 外泌體研究所、韓國中央大學醫學院皮膚科和美國關島皮膚病研究所共同進行的一項試驗,證實了人間充質干細胞來源的外泌體具有體外抗色素沉著作用和體內亮膚功效。相關研究成果發表在國際學術期刊《Cosmetics》上。

在這項研究中,研究人員發現外泌體都能降低細胞內黑色素水平,而沒有顯著的細胞毒性,外泌體的局部制劑減少了色素沉著過度。
治療 2 周,注意到測試治療區域和安慰劑對照區域之間黑色素水平降低的統計學顯著差異。然而,差異在治療 4 周后更明顯,并持續到治療后 8 周。

骨關節炎相關疾病方向的應用研究
外泌體作為良好的生物信號傳遞因子,具有更加強大的軟骨再生修復的應用潛能。
骨關節炎中,軟骨細胞通常表現出衰老特征,因此設法修復衰老的軟骨細胞可能成為有效的治療方案。
遵照這一思路,有研究者嘗試用來源于間充質干細胞的外泌體重新激活衰老的軟骨細胞。通過測序分析,研究者研究了間充質干細胞源性外泌體中的重要功能miRNA,并確認p53信號通路是其調控細胞衰老的關鍵信號通路。在通過細胞實驗證實了間充質干細胞源性外泌體對衰老軟骨細胞的作用后,作者引入軟骨細胞靶向肽,增加了間充質干細胞源性外泌體在軟骨部位的富集,同時,利用緩釋系統延長間充質干細胞源性外泌體在病變位置的作用時間,由此加強對骨關節炎的治療效果。此研究表明間充質干細胞來源的外泌體對異常的軟骨細胞代謝起到了積極作用。
間充質干細胞具有分化潛能高、移植后存活率高、無明顯不良反應等優點。它含有大量且種類繁多的蛋白質、細胞因子和生物活性物質。篇幅有限,以上只是外泌體在眾多疾病、問題方向的臨床研究中很小的一部分,外泌體在諸多研究中出色的表現,也讓我們看到它非常廣闊的的應用前景,也希望隨著科技的發展和研究的深入,外泌體可以在臨床應用,造福更多有需要的朋友。

齊魯細胞以標準化、良好表征,經過中檢院質量復核的臍帶間充質干細胞作為外泌體制備的種子細胞,基于標準化的細胞培養條件,自主研發了臨床級外泌體分離純化工藝,處理通量高、分離時間段、雜質去除率高。透射電子顯微鏡、蛋白標志物檢測、納米流式檢測以及NTA檢測結果顯示,外泌體的品質和純度均處于較高的水平。
【參考文獻】
[1]Embryonic stem cell-derived exosomes promote endogenous repair mechanisms and enhance cardiac function following myocardial infarction. Circ Res. 2015 Jun 19;117(1):52-64.
[2]xosomes in mesenchymal stem cells, a new therapeutic strategy for cardiovascular diseases? Int J Biol Sci. 2015 Jan 12;11(2):238-45.
[3]Circulating microRNAs are promising novel biomarkers of acute myocardial infarction. Intern Med. 2011;50(17):1789-95.
[4]Labusek N, Mouloud Y, K?ster C, Diesterbeck E, Tertel T, Wiek C, Hanenberg H, Horn PA, Felderhoff-Müser U, Bendix I, Giebel B, Herz J. Extracellular vesicles from immortalized mesenchymal stromal cells protect against neonatal hypoxic-ischemic brain injury. Inflamm Regen. 2023 Apr 17;43(1):24. doi: 10.1186/s41232-023-00274-6. PMID: 37069694; PMCID: PMC10108458.
[5] Zhao X, Fu L, Zou H, He Y, Pan Y, Ye L, Huang Y, Fan W, Zhang J, Ma Y, Chen J, Zhu M, Zhang C, Cai Y, Mou X. Optogenetic engineered umbilical cord MSC-derived exosomes for remodeling of the immune microenvironment in diabetic wounds and the promotion of tissue repair. J Nanobiotechnology. 2023 Jun 2;21(1):176. doi: 10.1186/s12951-023-01886-3. PMID: 37269014; PMCID: PMC10236791.



