發布時間:2022-11-04 瀏覽量:0

自2019年12月以來,新型冠狀病毒(COVID-19)在全球傳播迅速,造成了毀滅性的大流行,嚴重危害人們的健康。感染后,免疫系統被過度激活時會生成大量的炎癥因子,導致嚴重的細胞因子風暴,細胞因子風暴可導致肺及多器官損傷。輕者可表現為急性自限性癥狀,如發熱、乏力、干咳、流涕等,重者可出現急性呼吸窘迫綜合征、膿毒癥休克、出凝血功能障礙以及多器官功能障礙綜合征甚至死亡等。
細胞因子風暴是新冠肺炎患者輕癥向重癥和危重癥轉換的一個重要節點,有助于新冠肺炎的臨床分型以及預測發展的嚴重程度,并提供潛在的臨床靶標。
間充質干細(MSCs)是一類多潛能組織干細胞,在抗炎、再生、免疫調節等方面有著巨大潛力,能夠通過直接觸或旁分泌多種細胞因子的方式調節免疫,適時抑制過激免疫反應,抑制細胞因子風暴,同時具有促進損傷組織恢復的能力。

COVID-19具有獨特的免疫病理學,重癥COVID-19患者外周血CD4+和CD8+T淋巴細胞的數量常顯著減少,部分患者免疫系統因感染、藥物、自身免疫疾病等因素過度激活時,免疫細胞就會應激過度產生過多的TNF-α、IL-6、IL-10,TGF-β的分泌增加進而發展為急性呼吸窘迫綜合征,全身性炎癥反應綜合征,多器官功能障礙綜合征,導致全身性衰弱性疾病患者的死亡率增加。
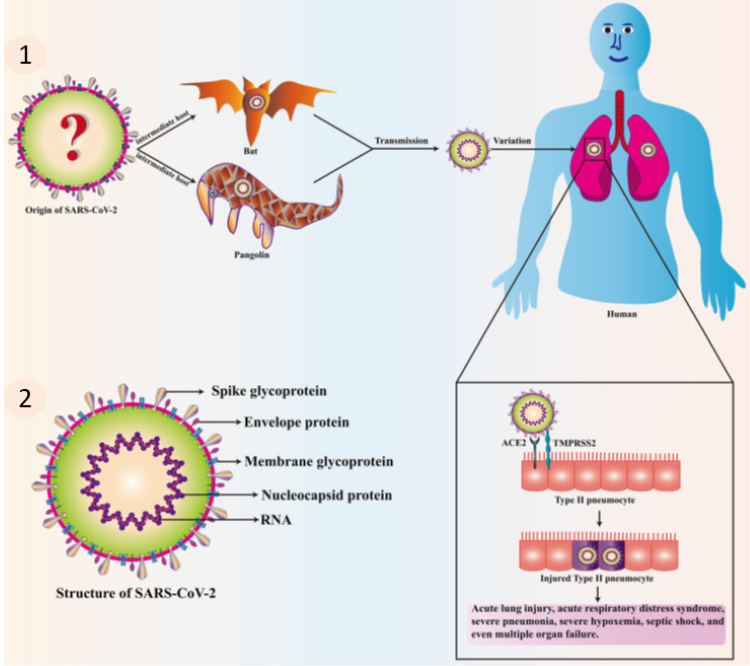
Figure1:新型冠狀病毒可能來源與進入宿主情況示意圖
Figure2:新型冠狀病毒結構示意圖

干細胞的臨床研究最終目標是通過刺激和調節內源性干細胞種群和/或補充細胞來增強機體修復機制,以達到組織穩態和再生的目的。干細胞療法受到了大量的臨床研究,并被定義為有潛力的藥物,為患有疾病的患者帶來了新的希望。

Figure3.干細胞研究進展時間表與來源示意圖
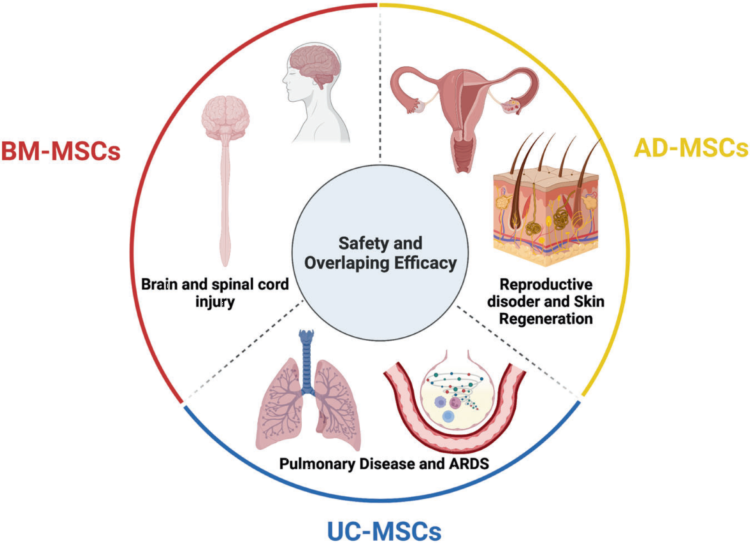
Figure4:不同干細胞研究方向示意圖

肺不成熟和肺纖維化是支氣管肺發育不良患者的主要問題,并導致SDF-1水平升高、纖維化的發展、炎癥反應的誘導和肺泡變性損傷。UC-MSCs通過化學引誘劑SDF-1被吸引到受損的肺,SDF-1和CXCR4的交流不斷地從未成熟的肺釋放。此外,UC-MSCs通過細胞間接觸機制降低促炎細胞因子(TGF-β、INF-γ、巨噬細胞MIF和TNF-α)的水平。UC-MSCs產生和分泌VEGF的能力也通過增強血管生成參與未成熟肺的再生。
慢性阻塞性肺疾病(COPD)加重時,UC-MSCs通過降低IL-8和TNF-α水平對周圍刺激作出反應,導致炎癥反應抑制,但增加參與肺泡保護、液體清除和減少氧化應激和肺纖維化的生長因子的分泌,包括HGF、TGF-β、IGF-1和外泌體。
UC-MSCs通過抑制2019冠狀病毒病(COVID-19)中細胞因子風暴的形成CD34+T細胞分化為Th17細胞并增加調節性T細胞數量。此外,UC-MSCs還通過分泌LL-3717和lipocalin具有抗菌活性。
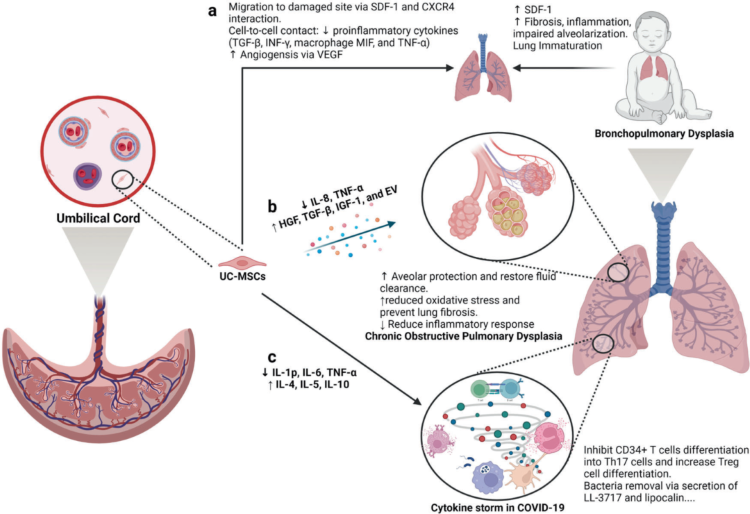
Figure5:UC-MSCs間充質干細胞作用機制示意圖

目前,有72項評估MSCs研究新型冠狀肺炎的安全性和有效性的臨床試驗在美國國立衛生研究院網登記注冊,并且其中30項已處于完成狀態。MSCs用于新冠肺炎患者臨床的相關研究仍處于摸索階段,Hashemian等的臨床試驗結果表明,多次、大劑量輸注同種異體產前來源(臍帶血與胎盤來源)的間充質干細胞是安全的,Meng等的一項1期臨床試驗中未觀察到嚴重的人臍帶血來源的間充質干細胞UC-MSCs輸注相關不良事件,表明靜脈輸注UC-MSCs是安全的,中、重度新冠肺炎患者耐受性良好。最近,在一項對100名重癥新冠肺炎患者的隨機、雙盲、對照的2期臨床試驗中發現,UC-MSCs對新冠肺炎所致的肺損傷是一種安全且潛在有效的研究方法。
MSCs在研究肺部疾病和肺炎患者中有多種潛在機制,包括調節免疫細胞功能、免疫調節、增強肺泡液清除和蛋白通透性、調節內質網應激和衰減肺纖維化。
總結目前的臨床研究表明:
1、MSCs針對急性呼吸窘迫綜合征、急性肺損傷、重癥肺炎、重癥新冠肺炎患者,已被證實具有良好的安全性和有效性;
2、MSCs是非常好的輔助手段,目前的文獻報道中未發生與MSCs直接相關的嚴重不良反應。
參考文獻:
[1] MENGF,XU R,WANG S,et al.Human umbilical cord-derivedmesenchymal stem cell therapy in patients with COVID-19: aphase 1 clinical trial[J].Signal Transduct Target Ther,2020,5( 1):172.
[2] HUANG C,WANG Y,LI X,et al. Clinical features of patientsinfected with 2019 novel coronavirus in Wuhan,China[J]. Lancet,2020,395( 10223):497–506.
[3] PROCKOPD J.The exciting prospects of new therapies with mesenchymalstromal cell[J].Cytotherapy,2017,19( 1):1–8.
[4] Lam, G., Zhou, Y., Wang, J. X. & Tsui, Y. P. Targeting mesenchymal stem celltherapy for severe pneumonia patients. World J. Stem Cells 13, 139–154(2021).
[5] Chen,K.etal. Human umbilical cord mesenchymal stem cells hUC-MSCs exertimmunosuppressive activities through a PGE2-dependent mechanism. Clin.Immunol. 135, 448–458 (2010).
[6] Ren, G. et al. Mesenchymal stem cell-mediated immunosuppression occurs viaconcerted action of chemokines and nitric oxide. Cell Stem Cell 2, 141–150(2008).
[7] Loy, H. et al. Therapeutic implications of human umbilical cord mesenchymalstromal cells in attenuating influenza A(H5N1) virus-associated acute lungnjury. J. Infect. Dis. 219, 186–196 (2019).
[8] Gazdhar, A. et al. Targeted gene transfer of hepatocyte growth factor to alveolartype II epithelial cells reduces lung fibrosis in rats. Hum. Gene Ther. 24, 105–116(2013).
[9] Wang, W. et al. Therapeutic mechanisms of mesenchymal stem cells in acuterespiratory distress syndrome reveal potentials for Covid-19 treatment. J. Transl.Med. 19, 198 (2021).
[10] Chu, K. A. et al. Reversal of bleomycin-induced rat pulmonary fibrosis by axenograft of human umbilical mesenchymal stem cells from Wharton’s jelly.Theranostics 9, 6646–6664 (2019)
[11] Lam, G., Zhou, Y., Wang, J. X. & Tsui, Y. P. Targeting mesenchymal stem celltherapy for severe pneumonia patients. World J. Stem Cells 13, 139–154(2021).
[12] Chen, K. et al. Human umbilical cord mesenchymal stem cells hUC-MSCs exertimmunosuppressive activities through a PGE2-dependent mechanism. Clin.Immunol. 135, 448–458 (2010).
[13] Ren, G. et al. Mesenchymal stem cell-mediated immunosuppression occurs viaconcerted action of chemokines and nitric oxide. Cell Stem Cell 2, 141–150(2008).
[14] Loy, H. et al. Therapeutic implications of human umbilical cord mesenchymalstromal cells in attenuating influenza A(H5N1) virus-associated acute lungnjury. J. Infect. Dis. 219, 186–196 (2019).
[15] Gazdhar, A. et al. Targeted gene transfer of hepatocyte growth factor to alveolartype II epithelial cells reduces lung fibrosis in rats. Hum. Gene Ther. 24, 105–116(2013).
[16] Wang, W. et al. Therapeutic mechanisms of mesenchymal stem cells in acuterespiratory distress syndrome reveal potentials for Covid-19 treatment. J. Transl.Med. 19, 198 (2021).
[17] Chu, K. A. et al. Reversal of bleomycin-induced rat pulmonary fibrosis by axenograft of human umbilical mesenchymal stem cells from Wharton’s jelly.Theranostics 9, 6646–6664 (2019)
[18] DucM,Hoang.etal.Stemcell based therapy for human diseases.Signal Transduction and Targeted Therapy(2022)7:272.