發布時間:2023-07-31 瀏覽量:0
特發性肺纖維化(IPF)患者數量逐步上升,但目前尚且缺乏有效的臨床手段。
特發性肺纖維化(IPF)是一種病因不明的慢性纖維化間質性肺疾病,目前最好的治療選擇仍然是肺移植[1]。IPF的特征是成纖維細胞在損傷部位分泌膠原蛋白,過多的結締組織沉積,肺中大量的瘢痕阻礙了肺泡和肺血管之間的氣體交換,導致肺功能的中斷,最終導致呼吸衰竭和死亡[2]。

近年來,細胞外囊泡(EVs)受到越來越多的關注,它在多種疾病中抗炎、抗纖維化和組織損傷修復等非凡的治療作用。更重要的是,EVs可以被修飾作為藥物或細胞因子遞送工具,靶向損傷部位以提高治療效果。因此,以肺微環境為目標的間充質干細胞-胞外囊泡(MSC-EVs)對IPF的治療策略為IPF的治療提供了新的思路。MSC-EVs現在被認為是比MSC移植更有效、更安全的替代方法,并在許多肺損傷和疾病的臨床前模型中顯示出良好臨床應用效果。
關于MSC-EV
EVs是由各種細胞分泌的磷脂雙分子層組成的膜性小囊泡,其中含有蛋白質、核酸和脂質。
到目前為止,細胞基本上釋放出三種EV亞型:外泌體、微囊泡(MVs)和凋亡小體,直徑分別為20-150nm、50-1000nm和大于1000 nm[4]。下表總結了EVs的特點。
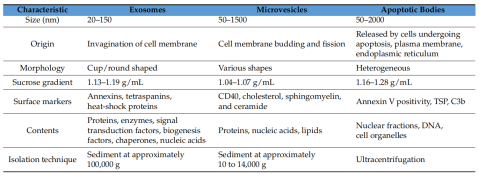
△ EVs的特點
EVs介導的細胞間通信依賴于細胞外囊泡的起源和受體細胞的來源。EVs通過轉移其所攜帶的生物分子物質,如蛋白質、脂質、mRNA和microRNA,來調節細胞反應,導致信號級聯,提醒或觸發靶細胞的生物過程,這使得囊泡可以在局部或在遠處與選定的靶細胞相互作用,并執行特定的生物學功能(見下圖)。
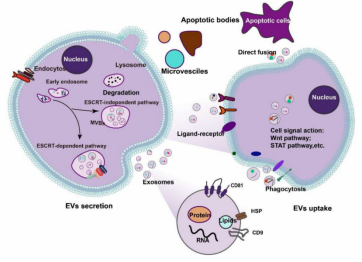
△細胞外囊泡(ev)的分泌和攝取
MSC-Ev的臨床應用機制
當IPF中損傷組織的愈合過程失時,會導致組織重塑、瘢痕組織形成異常和纖維化。病理性肺纖維化的主要部位是間質,包括肺泡上皮、肺毛細血管內皮、基底膜、血管周圍組織和淋巴組織。炎癥微環境和免疫調節失衡、ECM微環境改變等共同促進了IPF的發病機制。
臨床前研究表明,MSC-EVs在多種纖維化疾病中表現出抗纖維化和促進組織修復作用,主要機制是:
①在IPF中起抗炎作用;
②可調節IPF中的免疫反應;
③在IPF中調節ECM穩態。
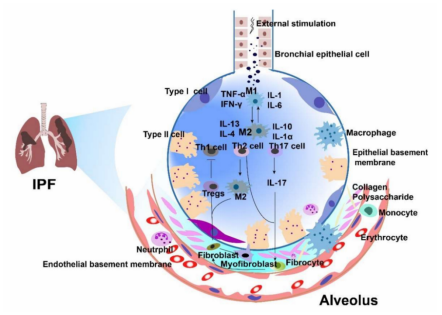
△特發性肺纖維化(IPF)微環境的穩態失衡
MSC-EVs治療IPF的策略
MSC-EVs治療IPF的治療策略主要有以下三種:
①MSC-EVs的全身遞送
②將MSC-EVs直接輸送到肺
③MSC-EVs作為IPF治療的靶向遞送載體
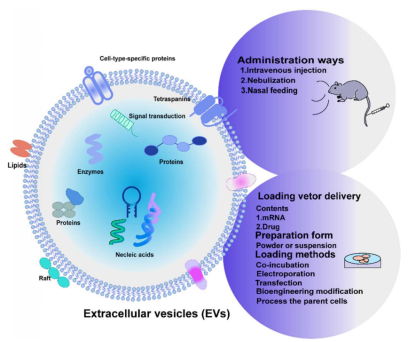
△MSC-EVs治療IPF的治療方式概述
MSC-Ev的治療挑戰
在IPF的動物模型中觀察到MSC-EVs吸入治療治療肺纖維化是有效的。但在其推向臨床中亟待解決一些問題:
①如何有效地將MSC-Ev傳遞至損傷部位;
②MSC-EVs的給藥劑量可能跟其治療場景有關;
③下肺中的表面活性劑有可能使脂質體和脂質納米顆粒不穩定。
④行業內還缺乏GMP生產方案及MSC-Ev缺少標準化。
截至到目前,通過Clinical Trials檢索到全球范圍內的MSCs臨床試驗研究項目已經超過4000多個。雖然通過一系列的臨床研究,發現MSCs在治療IPF方面有一定的優勢,但是在整個臨床應用中還是面臨著一定的挑戰,我們也相信隨著研究的深入以及科技的發展,這項技術一定會造福更多備受疾病困擾的朋友。
【參考文獻】
[1]Shenderov, K.; Collins, S.L.; Powell, J.D.; Horton, M.R. Immune dysregulation as a driver of idiopathic pulmonary fibrosis. J. Clin. Investig. 2021, 131, e143226.
[2]Betensley, A.; Sharif, R.; Karamichos, D. A Systematic Review of the Role of Dysfunctional Wound Healing in the Pathogenesis and Treatment of Idiopathic Pulmonary Fibrosis. J. Clin. Med. 2016, 6, 2.
[3]Gnecchi, M.; Danieli, P.; Malpasso, G.; Ciuffreda, M.C. Paracrine Mechanisms of Mesenchymal Stem Cells in Tissue Repair. Methods Mol. Biol. 2016, 1416, 123–146.
[4] Xu, R.; Greening, D.W.; Zhu, H.J.; Takahashi, N.; Simpson, R.J. Extracellular vesicle isolation and characterization: Toward clinical application. J. Clin. Investig. 2016, 126, 1152–1162.



