發(fā)布時(shí)間:2023-02-16 瀏覽量:0
2023年1月中旬,美國科研團(tuán)隊(duì)在《自然》子刊(Nature Reviews Microbiology)發(fā)布了篇與長新冠相關(guān)的研究綜述,研究顯示,長新冠是一種多系統(tǒng)疾病,包括慢性疲勞綜合征、自主神經(jīng)障礙,對多器官系統(tǒng)的影響以及血管和凝血異常。

近年來,關(guān)于如何修復(fù)新冠病毒感染后導(dǎo)致的肺部等系統(tǒng)損傷,科學(xué)家進(jìn)行了大量的嘗試。

香港瑪嘉烈醫(yī)院傳染病中心曾對首批出院病人進(jìn)行了跟蹤,結(jié)果發(fā)現(xiàn)有30%的康復(fù)者肺部功能受損兩至三成。感染后綜合征主要表現(xiàn)為步速較快時(shí)會(huì)氣促,無法正常做運(yùn)動(dòng),甚至不能做回以往的工作。
北京大學(xué)第一醫(yī)院感染疾病科主任王貴強(qiáng)指出,肺部嚴(yán)重感染會(huì)發(fā)展為肺纖維化,一部分重癥患者治愈后會(huì)出現(xiàn)肺纖維化,影響日常生活,發(fā)展到晚期只能肺移植。而且目前對于肺纖維化,還沒有特效藥,病情是不可逆轉(zhuǎn)的。
研究人員在一些從新冠中康復(fù)的患者中觀察到持續(xù)的氣流阻塞,造成肺部損傷。還可能出現(xiàn)另一種肺部疾病——肺擴(kuò)張障礙,減少肺部的容積,進(jìn)而減少肺部的吸入量。對于從新冠中康復(fù)的患者,特別是那些患有嚴(yán)重疾病的患者,以后可能發(fā)展為限制性肺部疾病。
新冠病毒感染導(dǎo)致的肺臟組織結(jié)構(gòu)破壞,還可能進(jìn)展為嚴(yán)重的呼吸窘迫綜合征 (Acute respiratory distress syndrome,ARDS)并最終導(dǎo)致呼吸衰竭,此為各類病毒性重癥肺炎患者死亡的最根本原因。
目前還沒有治療重癥及危重癥新冠肺炎的有效方法,但間充質(zhì)干細(xì)胞憑借其強(qiáng)大的免疫調(diào)節(jié)作用,被認(rèn)為是一種有前途的新型治療方法,雖然不是直接對抗病毒,但是可通過緩解炎癥反應(yīng),提高或恢復(fù)免疫力,以及借助多向分化潛能在肺部受損部位產(chǎn)生功能細(xì)胞,發(fā)揮修復(fù)功能,改善并提高重癥患者的生存率。也有研究認(rèn)為,這些免疫調(diào)節(jié)作用是由MSCs分泌的細(xì)胞外囊泡如外泌體介導(dǎo)的,可以有效減少細(xì)胞因子風(fēng)暴綜合征和ARDS的發(fā)生,以及降低肺纖維化水平,促進(jìn)組織損傷修復(fù)。

科學(xué)研究發(fā)現(xiàn),間充質(zhì)干細(xì)胞治療新冠具有巨大潛力。間充質(zhì)干細(xì)胞通過細(xì)胞直接接觸和旁分泌作用發(fā)揮免疫調(diào)節(jié)性能,抑制過度的免疫反應(yīng),對局部微環(huán)境內(nèi)穩(wěn)態(tài)起到維持作用,促進(jìn)組織的修復(fù),從而為炎癥相關(guān)性疾病和自身免疫性疾病等的治療提供新的治療策略。
外泌體是細(xì)胞外微囊泡的一種,里面包含有豐富的生物活性物質(zhì),如脂質(zhì)、蛋白、受體、以及RNA等。過去認(rèn)為細(xì)胞外微囊泡是細(xì)胞移除代謝廢物、維持細(xì)胞內(nèi)穩(wěn)態(tài)的一種機(jī)制,近年來研究揭示細(xì)胞外微囊泡還是細(xì)胞相互交流的一種重要方式。外泌體可以通過旁分泌或者內(nèi)分泌的方式作用于組織或者細(xì)胞。
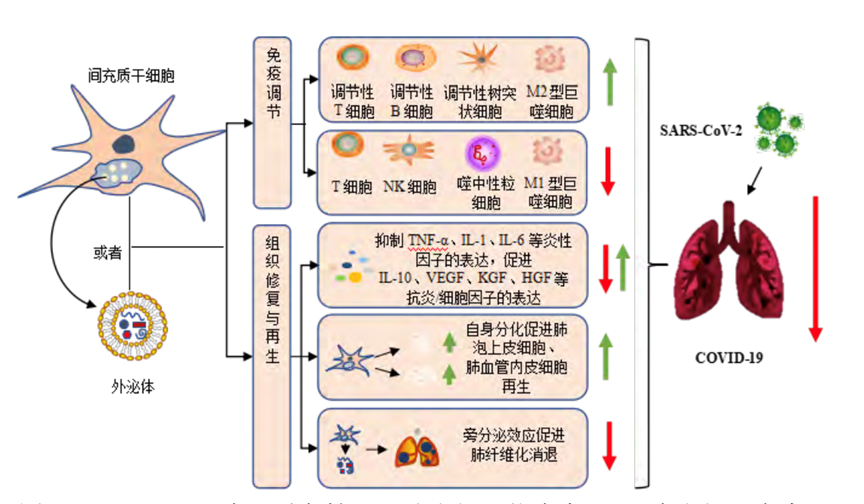
(圖片來源:間充質(zhì)干細(xì)胞及其外泌體治療——2019
冠狀病毒病的機(jī)遇與挑戰(zhàn);張雨晴,吳軍)
國內(nèi)外眾多醫(yī)學(xué)研究團(tuán)隊(duì)都對間充質(zhì)干細(xì)胞及其外泌體治療重癥COVID-19引起的呼吸窘迫和肺病問題的有效性和安全性做了研究和探討。
2021年8月,瑞金醫(yī)院呼吸與危重癥醫(yī)學(xué)科瞿介明教授團(tuán)隊(duì)團(tuán)隊(duì)首次驗(yàn)證經(jīng)霧化吸入異體人源間充質(zhì)基質(zhì)細(xì)胞外囊泡在臨床應(yīng)用中的可行性及安全性,相關(guān)研究成果刊發(fā)在國際頂級(jí)權(quán)威雜志Journal of Extracellular Vesicles(IF:25.841)上。

(圖片來源:Journal of Extracellular Vesicles
(IF:25.841))
2021年,發(fā)表在《Stem Cells and Development》上的一文指出,間充質(zhì)干細(xì)胞來源外泌體在治療重癥新冠肺炎患者成效顯著,康復(fù)率高達(dá)71%。外泌體具有安全性、恢復(fù)氧合、下調(diào)細(xì)胞炎癥因子和重建免疫系統(tǒng)功能等優(yōu)點(diǎn),是一種很有前途的新冠肺炎治療候選藥物。
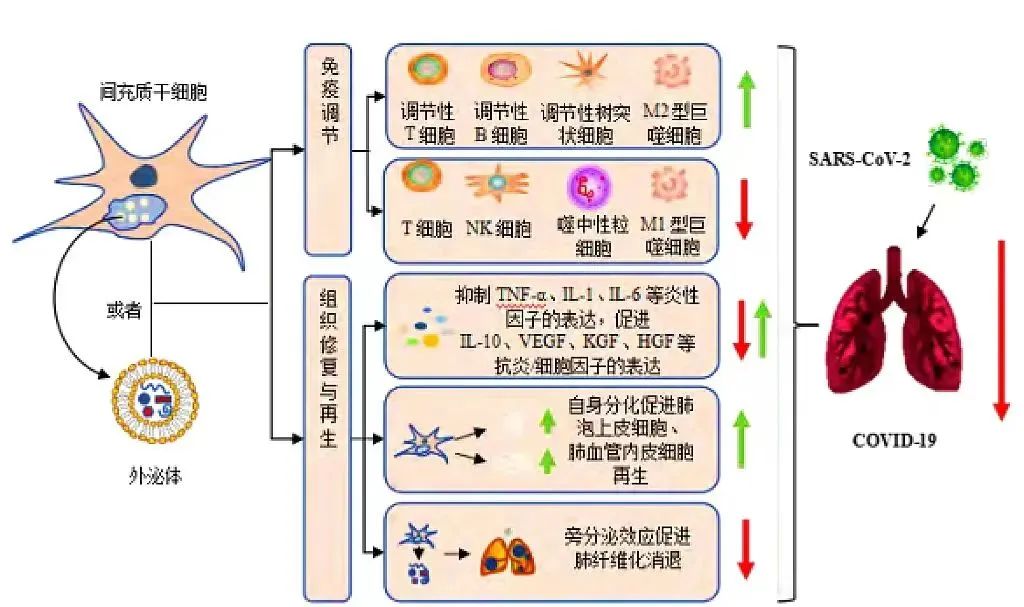
(間充質(zhì)干細(xì)胞及其外泌體治療 2019 冠狀病毒病
(COVID-19) 的主要調(diào)控機(jī)制)
2022年5月,有武漢、上海、北京三地學(xué)者共同發(fā)文,證實(shí)將干細(xì)胞外泌體以霧化形式吸入,能顯著改善重癥新冠肺炎患者的肺部損傷。
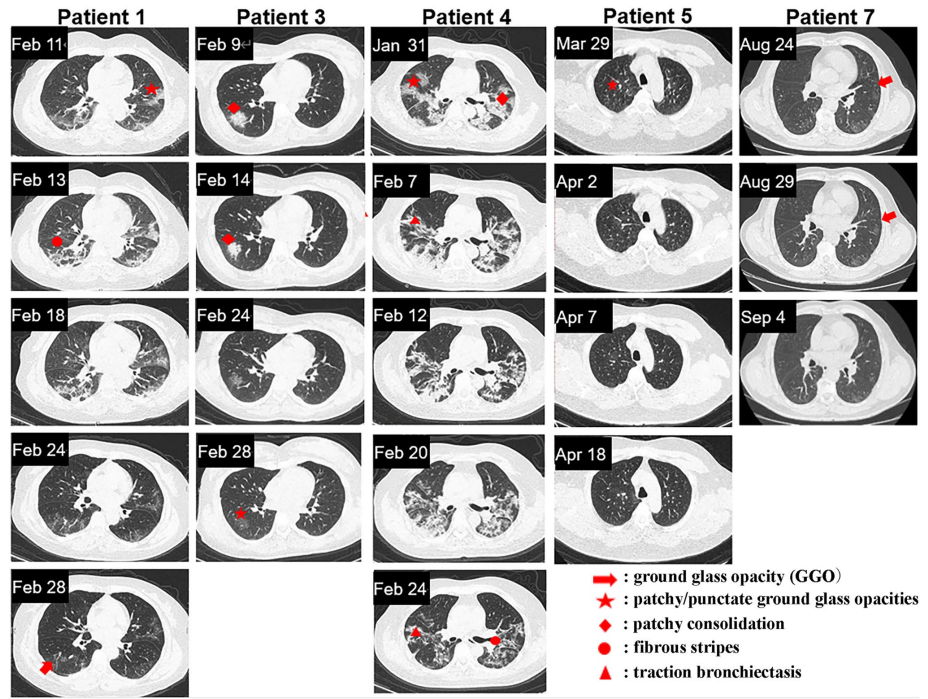
知名期刊《干細(xì)胞研究與治療》上刊載了一篇內(nèi)容,題為《Nebulized exosomes derived from allogenic adipose tissue mesenchymal stromal cells in patients with severe COVID-19: a pilot study》。研究者將源自人異體脂肪間充質(zhì)干細(xì)胞衍生的外泌體,以霧化吸入形式對7名重癥新冠肺炎患者進(jìn)行干預(yù),初步研究結(jié)果顯示參與者肺部損傷得到顯著改善。

(圖片來源:《Nebulized exosomes derived from allogenic adipose tissue mesenchymal stromal cells in patients with severe COVID-19: a pilot study》)
2022年,《Stem Cell Reviews and Reports》雜志(2022年影響因子6.692)發(fā)表了一項(xiàng)來自江蘇省無錫第五人民醫(yī)院的臨床研究,研究結(jié)果認(rèn)為,臍帶間充質(zhì)干細(xì)胞來源的外泌體霧化治療新冠肺炎安全可行。
(圖片來源:2022年《Stem Cell Reviews and Reports》)
外泌體的功能作用歸因于分泌它的細(xì)胞。MSCs分泌的外泌體攜帶了IL-10 mRNA、miR-126和miR-30b,它們可保護(hù)肺纖維化;同時(shí)還攜帶了各種免疫調(diào)節(jié)蛋白,包括血管生成素-1(Ang-1)和肝細(xì)胞生長因子(HGF),已知這兩種蛋白質(zhì)都能減輕動(dòng)物模型中的肺損傷。
霧化MSC來源的外泌體可以到達(dá)肺部的精細(xì)結(jié)構(gòu),如細(xì)支氣管和肺泡,以直接將抗炎分子遞送到它們的靶位,并且不會(huì)誘發(fā)急性過敏反應(yīng)或繼發(fā)性過敏反應(yīng),同時(shí)促進(jìn)肺部病變的吸收,并減少輕度新冠肺炎患者的住院時(shí)間。

整個(gè)臨床研究結(jié)果表明,不論是新冠病毒感染的重癥患者,還是輕癥患者,霧化吸入間充質(zhì)干細(xì)胞來源的外泌體能夠作為一種安全可行的新方法用于治療新冠病毒感染。
相信未來,干細(xì)胞以及干細(xì)胞外泌體的深入研究能為新冠肺炎的臨床治療提供更好的數(shù)據(jù)支持,期待實(shí)際應(yīng)用于社會(huì)化的新冠肺炎治療,更大程度的幫助全球疫情實(shí)現(xiàn)穩(wěn)定控制。

