發(fā)布時(shí)間:2021-05-14 瀏覽量:0
多發(fā)性骨髓瘤-“啃”骨頭的血癌
MULTIPLE MYELOMA
多發(fā)性骨髓瘤(MM)是僅次于非霍奇金淋巴瘤的第二大血液惡性腫瘤,其腫瘤細(xì)胞起源于骨髓中的漿細(xì)胞。特征為骨髓漿細(xì)胞異常增生,并且大部分伴有單克隆免疫球蛋白或輕鏈(M蛋白)過度生成,最終導(dǎo)致器官或組織損傷。MM常伴有多發(fā)性溶骨性損害、高鈣血癥、貧血、腎臟損害,因此也有人稱這種病為“啃”骨頭的血癌。
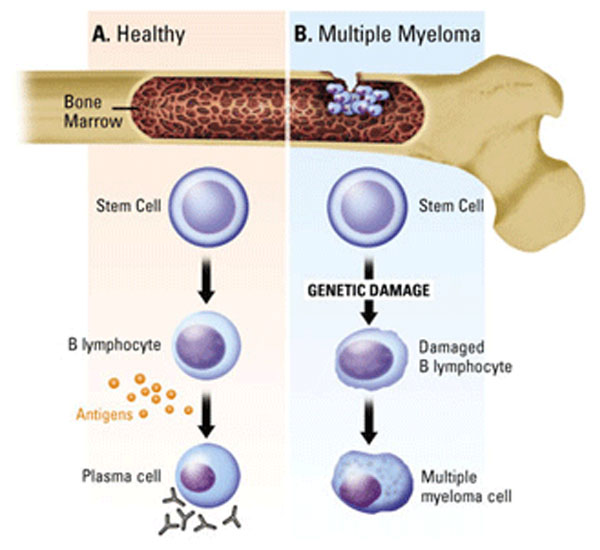
MM的治療經(jīng)歷了傳統(tǒng)的化療時(shí)期、造血干細(xì)胞移植時(shí)期、一直到目前的免疫抑制劑(如來(lái)那度胺)和蛋白酶體抑制劑(如卡非佐米)等為代表的新藥時(shí)期,MM患者的生存時(shí)期有所延長(zhǎng)。即使如此,MM在很大程度上依然是一種難以治愈的疾病,只有大約45%的患者在確診后能活過5年,許多患者最終會(huì)對(duì)現(xiàn)有療法產(chǎn)生耐藥,病情還會(huì)反復(fù)復(fù)發(fā)。所以到目前為止,MM仍被認(rèn)為是不可治愈的疾病,對(duì)新治療方法有著迫切需求。
隨著生物醫(yī)學(xué)及免疫學(xué)的發(fā)展,采用嵌合抗原受體(chimericantigenreceptor,CAR)修飾的T細(xì)胞的免疫治療以其驚人的療效迅速引起極大的關(guān)注。伴隨著2017年底兩款CAR-T細(xì)胞療法的獲批上市,這種新興的治療方式不僅得到了臨床治療效果的驗(yàn)證,同時(shí)也成為癌癥前沿治療領(lǐng)域的必爭(zhēng)之地。
靶向BCMA的CAR-T細(xì)胞療法
CELL THERAPY
B細(xì)胞成熟抗原(B-cellmaturationantigen,BCMA)正常表達(dá)于成熟的B細(xì)胞和漿細(xì)胞,在MM中也有廣泛的表達(dá),而不在人體主要器官的細(xì)胞中表達(dá),是一個(gè)非常理想的免疫治療靶點(diǎn)。
與CD19CAR-T治療方法的原理相似,BCMACAR-T細(xì)胞治療的原理是在患者的T細(xì)胞上嵌合BCMA的受體,從每例患者的血液中分離獲得T細(xì)胞,使用編碼BCMA抗原受體的慢病毒載體對(duì)T細(xì)胞進(jìn)行修飾,使T細(xì)胞表面表達(dá)BCMA受體。治療時(shí),MM患者先接受化療藥物預(yù)處理,以清除患者體內(nèi)現(xiàn)有的免疫細(xì)胞為CAR-T細(xì)胞留出生存和增殖的空間,隨后輸注BCMACAR-T細(xì)胞,一旦輸注回患者體內(nèi),BCMACAR-T就開始尋找并殺死表達(dá)BCMA的細(xì)胞。

2015年12月
美國(guó)NCI的JamesN.Kochenderfer,MD在美國(guó)血液病年會(huì)報(bào)道,利用anti-BCMA-CD28-CD3zeta載體構(gòu)建的CAR-T細(xì)胞,開展了12例患者的臨床試驗(yàn),其中,2例完全緩解(CR),1例部分反應(yīng)(VGPR),1例部分緩解(PR),5例SD;
2016年12月
Bluebirdbio(藍(lán)鳥公司)公布了其針對(duì)治療復(fù)發(fā)/難治性多發(fā)性骨髓瘤的bb2121的臨床1期試驗(yàn)中期數(shù)據(jù),顯示了這個(gè)以BCMA為靶點(diǎn)的CAR-T療法新產(chǎn)品的良好應(yīng)用前景。在整個(gè)臨床試驗(yàn)中,沒有出現(xiàn)劑量限制性毒性,患者經(jīng)歷1級(jí)和2級(jí)細(xì)胞因子釋放綜合征和1級(jí)神經(jīng)毒性。11例患者,不同的劑量梯度中,6個(gè)患者有響應(yīng),其中2例CR,1例VGPR,3例PR;
2018年12月
美國(guó)血液學(xué)會(huì)(ASH)上,南京傳奇和合作伙伴楊森提供了LEGEND-2(NCT03090659)I/II期開放標(biāo)簽研究的最新結(jié)果。57名晚期R/R多發(fā)性骨髓瘤患者接受了LCAR-B38MCAR-T細(xì)胞治療,ORR為88%。其中,74%的患者達(dá)到CR,4%的患者達(dá)到非常好的VGPR,11%的患者達(dá)到部分反應(yīng)PR;
2019年
NoopurRaje等報(bào)道了其針對(duì)治療復(fù)發(fā)/難治性多發(fā)性骨髓瘤的bb2121的臨床1期試驗(yàn)數(shù)據(jù),ORR為85%,包括15例(45%)CR。
目前已獲批上市的BCMACAR-T療法
BMACAR-TTHERAPY
2021年3月27日,全球首款以BCMA為靶點(diǎn)的CAR-T細(xì)胞經(jīng)由美國(guó)FDA批準(zhǔn)用于治療接受過四種以上前期療法的復(fù)發(fā)/難治性多發(fā)性骨髓瘤(r/rMM)成年患者。此款新的CAR-T細(xì)胞療法由百時(shí)美施貴寶(BMS)和bluebirdbio(藍(lán)鳥)聯(lián)合開發(fā),其產(chǎn)品名稱為Abecma(idecabtagenevicleucel;ide-cel)。
ide-cel獲批主要基于關(guān)鍵II期臨床試驗(yàn)的結(jié)果。該研究中,127例先前接受過至少3種療法且對(duì)最后一種療法無(wú)效的過度預(yù)治療復(fù)發(fā)和難治性多發(fā)性骨髓瘤患者接受了ide-cel劑量水平為300-460x10E6CAR+T細(xì)胞治療。
在接受治療后可評(píng)估療效的患者中,所有劑量水平的總緩解率(ORR)為72%,其中28%的患者獲得完全緩解(CR)或嚴(yán)格緩解(sCR)。治療后起效的中位時(shí)間是30天,中位緩解持續(xù)時(shí)間(DoR)達(dá)11個(gè)月,有CR或sCR的患者中位DOR為19.0個(gè)月。
與CD19CAR-T細(xì)胞療法的副作用相似,BCMACAR-T細(xì)胞療法也會(huì)出現(xiàn)兩種副作用—細(xì)胞因子釋放綜合征(CRS)和神經(jīng)毒性,此產(chǎn)品的整體安全性良好,CRS的3級(jí)及以上不良反應(yīng)的發(fā)生率為9%,神經(jīng)毒性的3級(jí)及以上不良反應(yīng)的發(fā)生率為4%。
齊魯細(xì)胞BCMA CAR-T項(xiàng)目研發(fā)
RESEARC AND DEVELOPMENT
本公司致力于CAR-T領(lǐng)域的研發(fā),尤其是靶向CD19的CAR-T細(xì)胞,在臨床研究中達(dá)到了很好的治療效果,當(dāng)然對(duì)于當(dāng)前熱門的BCMACAR-T的研發(fā)也是早有布局。從質(zhì)粒生產(chǎn)、慢病毒載體制備、CAR-T細(xì)胞制備、質(zhì)量研究等均為自主研發(fā)。

目前本公司已與醫(yī)院合作開展BCMA CAR-T療法的臨床研究,隨訪期內(nèi)患者全部處于完全緩解期,雖然有一定的副作用,但都在可控范圍。相信隨著技術(shù)的進(jìn)步和時(shí)間的推移,CAR-T療法會(huì)給患者帶來(lái)更好的治療效果。