發布時間:2024-09-26 瀏覽量:0

在過去幾十年中,干細胞研究的數量呈指數級增長。其中,2018年是MSC治療領域的一個里程碑,歐洲醫療機構(EMA)首次批準了MSC產品的上市。
2018年9月,歐洲一公司宣布其三期實驗(NCT02336230)的陽性結果,該實驗使用同種異體骨髓(BM)間充質干細胞(remestemcel-l)治療類固醇難治性急性GVHD兒童,實驗結果可以向美國食品和藥物管理局(FDA)申請使用許可證。
因此,2019年將是MSC治療時代的開始。但不同MSCs產品會造成不同治療效果:
(1)針對GVHD適應癥,Mesoblast 公司開展的3期臨床試驗(NCT00366145)中,Remestemcel-L是來自1個供體擴增至3-4代的MSCs,以滿足240名受試者的使用需求。臨床試驗結果比較積極,但未能達到主要臨床終點。
(2)同樣是針對GVHD適應,法蘭克福大學醫院開展的2期臨床試驗中,使用了來自8個供體混合的1-2代 MSCs,治療26名患者,取得了77%的總緩解率。
不同的臨床結果的原因,是因為MSCs產品的異質性(供體不同,細胞代次不同,工藝不同),還是因為受試者疾病個體化差異造成的?需要肯定的是:如果干細胞采用自動化制備,既可減少制備過程中的人為操作因素,也能降低產品異質性風險。基于此必須提出MSC異質性的概念。
關于細胞的異質性
PART 01
細胞的異質性(heterogeneity)是一個普遍存在的生物學現象,貼壁培養的MSC是由一個混合的細胞群體所組成,存在不同的細胞亞群(如克隆大小不一),有些亞群的細胞具有多潛能特性,有些亞群的細胞具有單潛能特性。
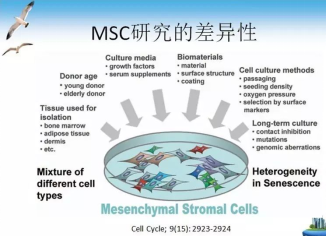
為什么MSC會存在異質性
PART 02
不同部位和不同個體來源的MSC都存在功能和形態上的一些差異。功能的差異在于功能的強弱不同或細胞因子表達譜的差異,例如所有MSC都具有免疫抑制功能,但是不同組織和不同個體來源的MSC,在免疫抑制功能上存在強弱之分。
其次,采樣方式也導致了MSC的異質性。AD-MSC是MSC異質性的一個示例。與組織塊切除相比,通過脂吸能獲得更高的活AD-MSC產量。與激光輔助抽脂和手術活檢相比,動力輔助抽脂方法對分離的AD-MSC具有更高的增殖潛能和抗衰老能力。此外,微套管微抽吸脂肪比通常的方法更有效,如更高的產量、更強的活力、更好的粘附率和更大的生長因子分泌量。在采樣方式方面表現出差異的其他MSC類型是UC-MSC。
不過因供體來源、細胞培養方案、保存條件而引起的MSC異質性相對可控,可通過制定分離、擴增等標準進行規范。關于這方面的規范,2021年頒布實施的人間充質干細胞團體標準(T/CSCB 0030-2021)也給出了相應的參考。

此外,MSC的組織來源多種多樣,在骨髓、脂肪、臍帶、心臟等多種組織中均能分離得到,這些不同組織器官分離得到的MSC雖然都符合2006年國際細胞治療學會制定的MSC最低鑒定標準,但它們的功能并不相同,即存在功能異質性。例如,臍帶來源的MSC表現出更好的體外擴增能力,但其成脂分化能力弱于骨髓來源的MSC;組織起源不同引起的MSC異質性相對復雜,對于解決MSC療效的不穩定性而言是一個更本源的問題,因此也是目前科學家們著力研究的方向。
如何減少MSC異質性?
PART 03
為了盡可能避免因組織起源不同而引起的MSC異質性,以獲得質量更為穩定、性質更為均一的MSC亞群,目前主要有兩種思路,一種是表面標志物篩選,通過流式細胞術篩選出具有特定表面標志物(如CD73、CD90、CD105)的細胞,以確保培養中使用的細胞群體具有均一性,例如免疫磁珠分選:使用免疫磁珠技術分選出目標細胞群體,提高細胞純度和功能一致性。但這些標志物的篩選和驗證目前大多基于動物模型的研究結果,與人存在一定的物種差異,有待進一步驗證。因此,根據特定標志物來區分不同組織MSC及其功能亞群的研究還有很長的路要走。
二是基因編輯技術:使用CRISPR/Cas9等基因編輯技術,修飾與細胞老化相關的基因(如p53、p16、p21),以延緩細胞老化。或基因修飾技術:通過基因修飾,過表達抗衰老相關基因(如hTERT)或抑制衰老相關基因表達,可以延長MSCs的壽命和功能。

除此之外,通過探究MSC的發育起源,在體外限定MSC的分化方向,以獲得來源限定的MSC是提升MSC均質性的另一種思路。現有研究結果表明,不同組織器官來源MSC的發育起源并不完全一致。由于中胚層可以發育成為機體的真皮、骨骼、肌肉、心臟和骨髓等組織器官,因而傳統觀點認為,骨髓MSC的發育起源是中胚層。然而,Isern等人在利用Nestin-GFP+小鼠模型研究時發現,在胎鼠圍產期骨髓中發現了兩種不同起源的MSC。除中胚層起源的MSC外,還有一群起源于軀干神經嵴(neural crest,NC)的MSC,且這兩種MSC表現出不同的生物學特性和功能。起源于中胚層的MSC在軟骨內骨化方面占據優勢,而神經嵴起源的MSC則表現出良好的支持造血方面的功能。
因此,我們需要開發出相應的方法學來為特定的疾病尋找具有特定治療能力的MSC,使其功能最大化。
【注】文章內容旨在科普細胞知識,進行學術交流分享,了解行業前沿發展動態。


